El uso de parche transdérmico de estradiol no se recomienda actualmente para pacientes pediátricos debido a la falta de datos establecidos sobre seguridad y eficacia.Las directrices normativas y las pruebas clínicas no respaldan su uso en niños, ya que los riesgos -incluidos los posibles efectos hormonales y sobre el desarrollo- siguen sin estudiarse en esta población.Los tratamientos alternativos con perfiles de seguridad pediátrica probados deben considerarse bajo supervisión médica.

Explicación de los puntos clave:
-
Falta de indicación pediátrica
- Las formulaciones transdérmicas de estradiol (parche, gel, aerosol) no están aprobadas por la FDA ni validadas clínicamente para niños.
- La ausencia de estudios controlados significa que se desconocen los posibles efectos secundarios (por ejemplo, alteración hormonal, interferencia en el crecimiento).
-
Problemas de seguridad y eficacia
- La fisiología pediátrica (p. ej., tasas metabólicas, absorción cutánea) difiere de la de los adultos, lo que aumenta la imprevisibilidad de la respuesta al fármaco.
- Medicamentos transdérmicos análogos (por ejemplo, selegilina) han mostrado riesgos como ideación suicida en pacientes más jóvenes, subrayando la necesidad de precaución.
-
Orientaciones normativas y clínicas
- El etiquetado actual indica explícitamente que estos productos no están indicados para uso pediátrico.
- Un uso no indicado sin pruebas sólidas podría exponer a los niños a riesgos innecesarios.
-
Enfoques alternativos
- Para las afecciones que requieren terapia estrogénica (por ejemplo, retraso puberal), los endocrinólogos pediátricos suelen optar por formas orales o inyectables con protocolos de dosificación establecidos.
- Para equilibrar los beneficios terapéuticos con las repercusiones en el desarrollo, es esencial un estrecho seguimiento.
Aunque la administración transdérmica ofrece comodidad, su aplicación en pediatría exige una investigación rigurosa.Hasta que se disponga de estos datos, los médicos deben dar prioridad a los tratamientos con perfiles de seguridad documentados para los pacientes más jóvenes.
Tabla resumen:
| Preocupación clave | Explicación |
|---|---|
| Falta de indicación pediátrica | No aprobado por la FDA para niños; no hay estudios controlados sobre seguridad o eficacia. |
| Riesgos de seguridad | Posible alteración hormonal, interferencia en el crecimiento y absorción impredecible. |
| Orientación reglamentaria | El etiquetado excluye explícitamente el uso pediátrico debido a riesgos no estudiados. |
| Alternativas | Terapias con estrógenos orales o inyectables con dosificación pediátrica establecida. |
Para obtener asesoramiento experto sobre soluciones de terapia hormonal pediátrica, póngase en contacto con Enokon hoy mismo .Como fabricante a granel de confianza de parches transdérmicos y apósitos para el dolor, estamos especializados en I+D a medida para distribuidores farmacéuticos y marcas del sector sanitario.Permítanos ayudarle a desarrollar soluciones seguras y eficaces adaptadas a sus necesidades.
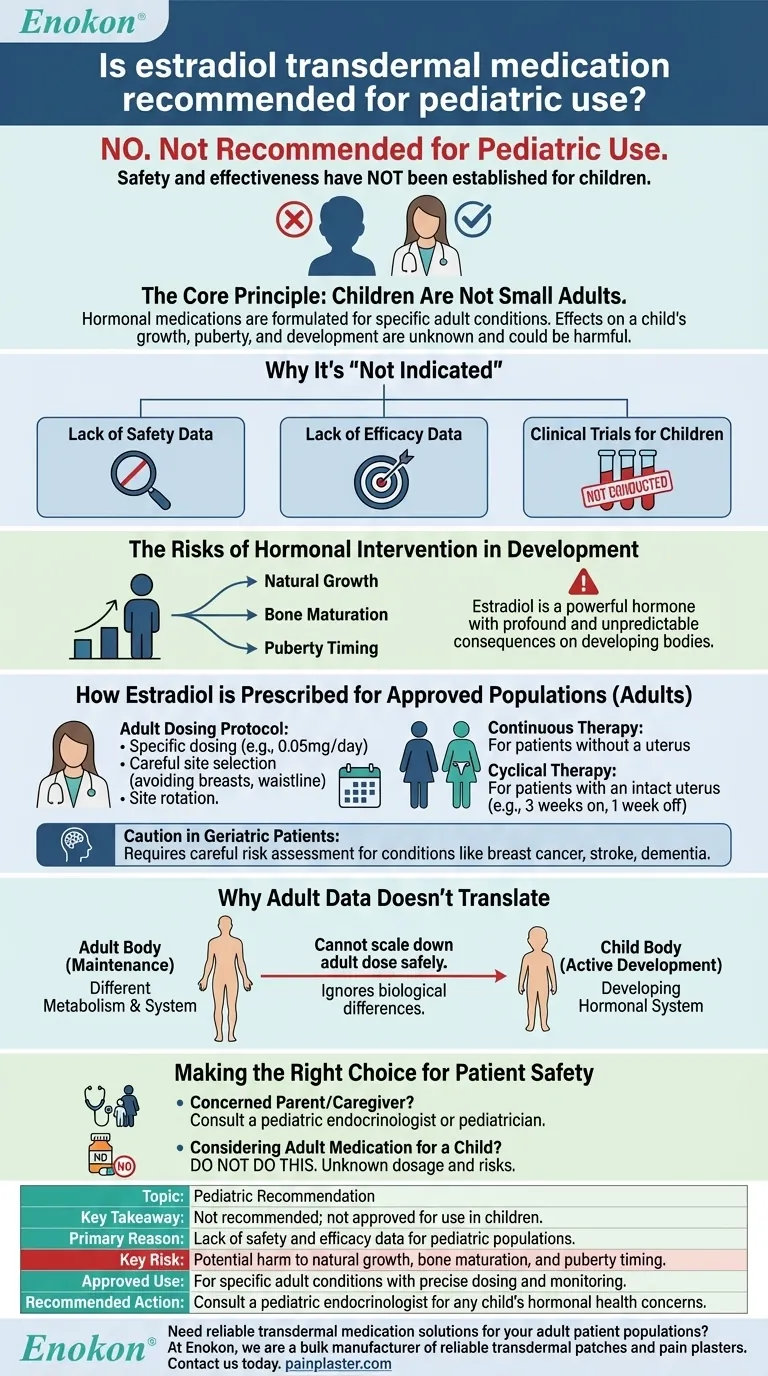
Guía Visual
Productos relacionados
- Calor infrarrojo lejano Parches analgésicos Parches transdérmicos
- Parche analgésico de gel mentolado
- Parche analgésico Icy Hot Menthol Medicine
- Parche de silicona para cicatrices Parche transdérmico para medicamentos
- Parche analgésico de artemisa y ajenjo para el dolor de cuello
La gente también pregunta
- ¿Cuál es el propósito de la filtración por vacío para soluciones poliméricas? Garantizar la calidad en la fabricación de parches transdérmicos
- ¿Qué papel juega un desecador en el análisis del contenido de humedad de los parches transdérmicos? Garantizar la estabilidad y la seguridad
- ¿Pueden convertirse todos los medicamentos en formas transdérmicas? Comprender los límites de la administración cutánea
- ¿Cómo mejoran los parches transdérmicos el cumplimiento de la medicación?Facilitan el cumplimiento del tratamiento
- ¿Qué papel juegan los parches transdérmicos en la mejora de las lesiones cutáneas? Descubra cómo la estabilización previene las úlceras por presión