El intervalo de edad aprobado para el uso de clonidina transdérmica es a partir de los 18 años.No está aprobada explícitamente para menores de 18 años.El parche transdérmico de clonidina fue aprobado por la FDA en 1984 para el tratamiento de la hipertensión de leve a moderada, sola o con un diurético, y funciona como un agente hipotensor alfa-agonista de acción central.
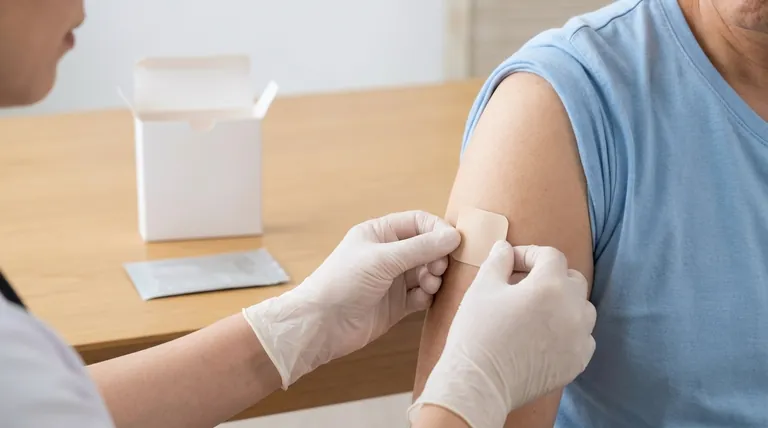
Explicación de los puntos clave:
-
Restricción de edad aprobada por la FDA
- Clonidina transdérmica no está aprobada para pacientes menores de 18 años .Esta restricción se repite en múltiples referencias, subrayando su importancia en el uso clínico.
- El parche está indicado específicamente para adultos (mayores de 18 años), probablemente debido a la insuficiencia de datos sobre seguridad/eficacia en poblaciones pediátricas o a los riesgos potenciales exclusivos de los pacientes más jóvenes.
-
Uso médico principal
- Aprobado para tratar hipertensión de leve a moderada (tensión arterial alta), como monoterapia o combinado con un diurético.
- Su mecanismo consiste en actuar como agonista alfa de acción central que reduce la actividad del sistema nervioso simpático para disminuir la presión arterial.
-
Antecedentes normativos
- La FDA aprobó la formulación transdérmica en 1984 lo que refleja el papel que desempeña desde hace tiempo en el tratamiento de la hipertensión.
- La limitación de edad se ha mantenido constante desde su aprobación, lo que sugiere que no existen pruebas posteriores que apoyen su uso pediátrico.
-
Consideraciones clínicas para los compradores
- Los profesionales sanitarios que adquieran el parche deben verificar la edad del paciente para evitar el uso no indicado en niños.
- La restricción implica que pueden ser necesarias terapias antihipertensivas alternativas para los pacientes pediátricos.
Esta claridad garantiza el cumplimiento de las directrices de prescripción y la seguridad del paciente.Para la población adulta, el parche ofrece una opción no oral para el control de la presión arterial, un detalle valioso para los responsables de la toma de decisiones en materia de formulación.
Tabla resumen:
| Aspecto clave | Detalles |
|---|---|
| Edad aprobada | A partir de 18 años (no para uso pediátrico) |
| Uso primario | Tratamiento de la hipertensión de leve a moderada |
| Mecanismo de acción | Alfa-agonista de acción central para reducir la presión arterial |
| Año de aprobación por la FDA | 1984 |
| Consideraciones clínicas | Verificar la edad del paciente; se necesitan terapias alternativas para pacientes menores de 18 años |
¿Necesita soluciones transdérmicas fiables para el tratamiento de la hipertensión en adultos?
Enokon está especializada en la fabricación a granel de parches transdérmicos de alta calidad, incluidas fórmulas de clonidina, para distribuidores sanitarios y marcas farmacéuticas.Nuestra experiencia garantiza el cumplimiento de las directrices de la FDA y una integración perfecta en su línea de productos.
Póngase en contacto con nosotros para hablar de I+D a medida, pedidos al por mayor o apoyo normativo: mejoremos juntos la atención al paciente.
Guía Visual
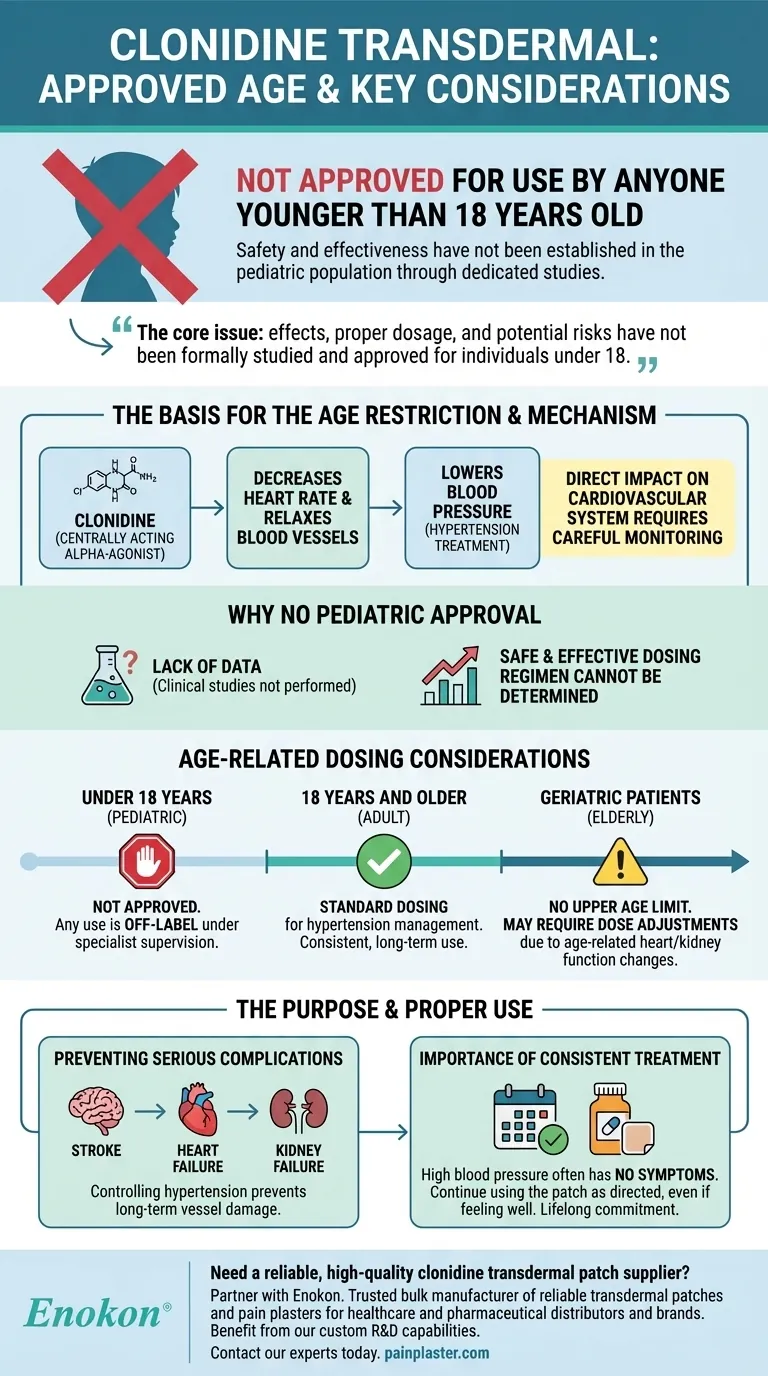
Productos relacionados
- Calor infrarrojo lejano Parches analgésicos Parches transdérmicos
- Parche de silicona para cicatrices Parche transdérmico para medicamentos
- Parche analgésico Icy Hot Menthol Medicine
- Parche analgésico de gel mentolado
- Parche analgésico de artemisa y ajenjo para el dolor de cuello
La gente también pregunta
- ¿Qué ventajas clínicas ofrecen los parches transdérmicos a los pacientes ancianos?Optimice la atención geriátrica con facilidad
- ¿Cómo contribuye el polvo cerámico de infrarrojos lejanos de alta pureza a la eficacia de los parches de fisioterapia de infrarrojos lejanos?
- ¿Cuáles son las principales ventajas de utilizar parches transdérmicos?Descubra las ventajas de la administración de medicamentos sin dolor
- ¿Cómo mejoran los parches transdérmicos el cumplimiento de la medicación?Facilitan el cumplimiento del tratamiento
- ¿Qué papel juegan los parches transdérmicos en la mejora de las lesiones cutáneas? Descubra cómo la estabilización previene las úlceras por presión











