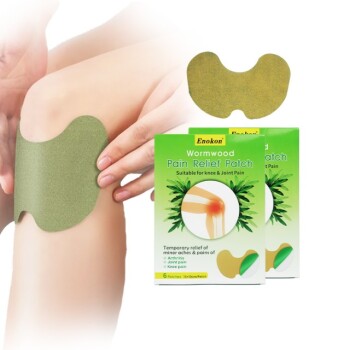
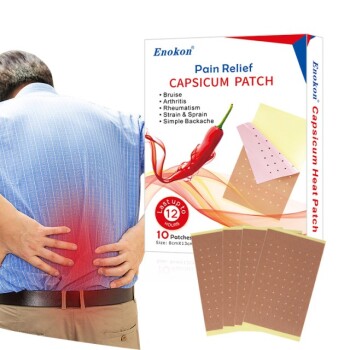
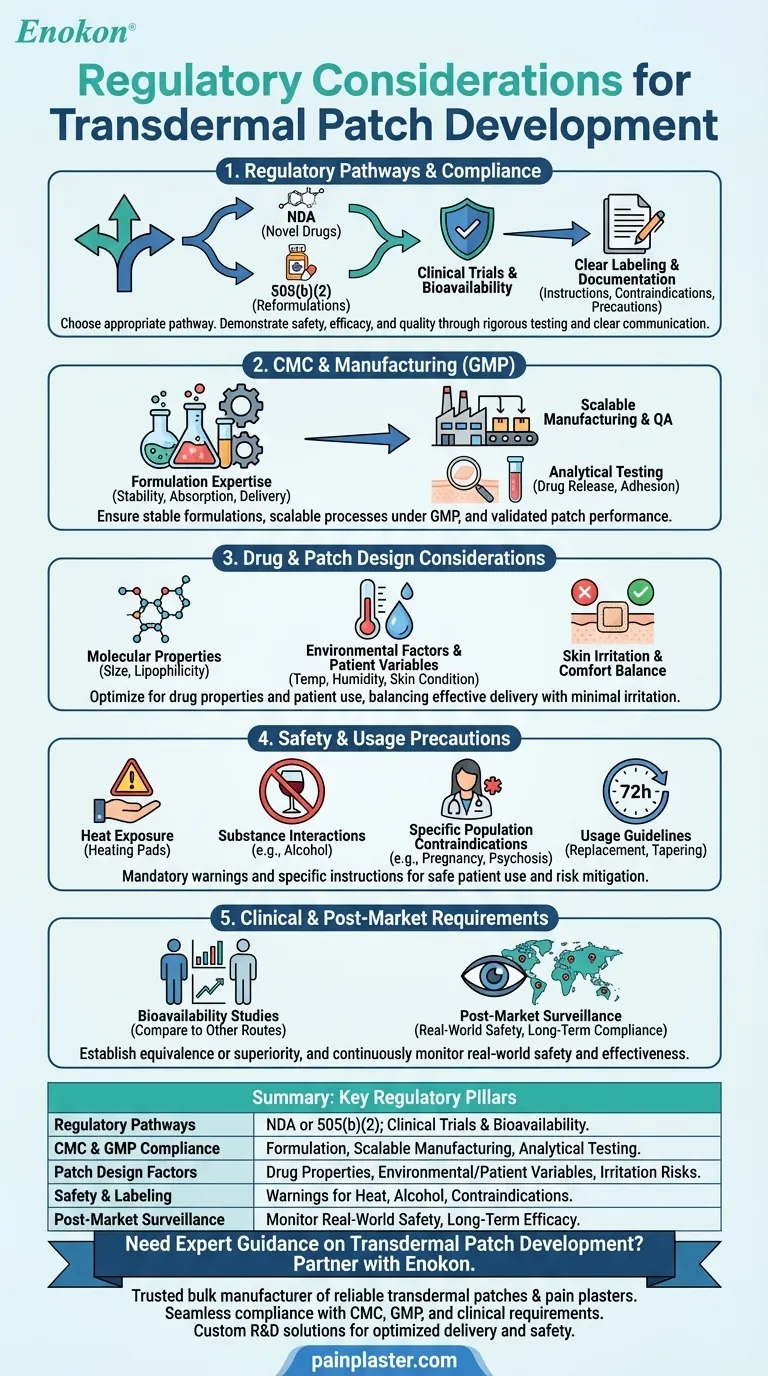
El desarrollo de parches transdérmicos implica navegar por un complejo panorama normativo para garantizar la seguridad, la eficacia y la calidad.Entre las consideraciones clave figuran el cumplimiento de los requisitos químicos, de fabricación y de control (CMC), la observancia de las Buenas Prácticas de Fabricación (BPF) y la realización de pruebas clínicas exhaustivas de biodisponibilidad y seguridad.El diseño del parche debe tener en cuenta las propiedades del fármaco (por ejemplo, tamaño molecular, polaridad) y los factores ambientales, mientras que el etiquetado y la documentación deben cumplir normas estrictas.En función de la novedad del fármaco, pueden aplicarse vías reguladoras como la NDA o el 505(b)(2).Precauciones como los riesgos de irritación cutánea y las restricciones de uso (por ejemplo, evitar la exposición al calor) también deben abordarse para obtener la aprobación y garantizar la seguridad del paciente.

Explicación de los puntos clave:
-
Vías reglamentarias y cumplimiento
- Los promotores deben elegir entre una solicitud de nuevo fármaco (NDA) para fármacos nuevos o una vía 505(b)(2) para reformulaciones de fármacos aprobados.
- Cumplimiento de parches transdérmicos exige demostrar la seguridad, eficacia y calidad mediante ensayos clínicos, incluidos estudios de biodisponibilidad.
- Es obligatorio que el etiquetado y la documentación sean claros y detallen las instrucciones de uso, las contraindicaciones (por ejemplo, la psicosis relacionada con la demencia) y las precauciones (por ejemplo, evitar el alcohol o la exposición al calor).
-
Química, fabricación y controles (CMC)
- La experiencia en formulación es fundamental para garantizar la estabilidad del fármaco, su absorción y unos índices de administración constantes.
- La escalabilidad y la garantía de calidad durante la fabricación comercial deben ajustarse a las normas BPF.
- Las pruebas analíticas validan el rendimiento del parche, incluidos los perfiles de liberación del fármaco y las propiedades de adhesión.
-
Consideraciones sobre el fármaco y el diseño del parche
- Las propiedades moleculares (por ejemplo, tamaño pequeño, lipofilia) influyen en las tasas de absorción y deben optimizarse durante el desarrollo.
- Los factores ambientales (temperatura, humedad) y las variables específicas del paciente (estado de la piel, edad) afectan a la eficacia y requieren ensayos en condiciones realistas.
- Los parches deben equilibrar la administración del fármaco con la comodidad, minimizando la irritación de la piel o las reacciones alérgicas.
-
Precauciones de seguridad y uso
- El etiquetado debe advertir de riesgos como la irritación de la piel, la exposición al calor (por ejemplo, almohadillas térmicas) y las interacciones con sustancias como el alcohol.
- Las poblaciones específicas (embarazadas/enfermeras, personas con psicosis) pueden requerir contraindicaciones.
- Las directrices de uso (por ejemplo, sustitución cada 72 horas, protocolos de disminución progresiva) deben comunicarse claramente a los pacientes.
-
Requisitos clínicos y posteriores a la comercialización
- Los estudios de biodisponibilidad comparan la administración transdérmica con otras vías (por ejemplo, la oral) para establecer la equivalencia o superioridad.
- La vigilancia posterior a la comercialización controla la seguridad en el mundo real, garantizando el cumplimiento a largo plazo y abordando los efectos adversos imprevistos.
Al abordar estas áreas, los desarrolladores pueden sortear los obstáculos normativos y, al mismo tiempo, ofrecer terapias transdérmicas eficaces y cómodas para el paciente.¿Se ha planteado cómo podrían evolucionar los adhesivos de los parches para reducir la irritación de la piel sin comprometer la administración del fármaco?
Tabla resumen:
| Principales consideraciones reglamentarias | Detalles |
|---|---|
| Vías reglamentarias | NDA para nuevos medicamentos; 505(b)(2) para reformulaciones.Requiere ensayos clínicos y estudios de biodisponibilidad. |
| Cumplimiento de CMC y GMP | Estabilidad de la formulación, fabricación escalable y pruebas analíticas (liberación del fármaco, adhesión). |
| Factores de diseño del parche | Optimizar las propiedades del fármaco (tamaño, lipofilia), las variables ambientales/paciente y los riesgos de irritación cutánea. |
| Seguridad y etiquetado | Advierta sobre la exposición al calor, las interacciones con el alcohol y las contraindicaciones para poblaciones de alto riesgo. |
| Vigilancia posterior a la comercialización | Supervise la seguridad en el mundo real y la eficacia a largo plazo tras la aprobación. |
¿Necesita asesoramiento experto sobre el desarrollo de parches transdérmicos? Asóciese con Enokon es un fabricante de confianza de parches transdérmicos y apósitos analgésicos para marcas y distribuidores del sector sanitario.Nuestra experiencia técnica garantiza el cumplimiento sin fisuras de los requisitos CMC, GMP y de pruebas clínicas, mientras que nuestras soluciones de I+D personalizadas optimizan la administración de fármacos y la seguridad del paciente. Póngase en contacto con nosotros para hablar de su proyecto.
Guía Visual
Productos relacionados
- Calor infrarrojo lejano Parches analgésicos Parches transdérmicos
- Parche de silicona para cicatrices Parche transdérmico para medicamentos
- Parche analgésico Icy Hot Menthol Medicine
- Parche analgésico de gel mentolado
- Parche analgésico de artemisa y ajenjo para el dolor de cuello
La gente también pregunta
- ¿Pueden convertirse todos los medicamentos en formas transdérmicas? Comprender los límites de la administración cutánea
- ¿Cuáles son las desventajas de la administración transdérmica de fármacos?Principales limitaciones a tener en cuenta
- ¿Qué papel juega un desecador en el análisis del contenido de humedad de los parches transdérmicos? Garantizar la estabilidad y la seguridad
- ¿Qué papel juegan los parches transdérmicos en la mejora de las lesiones cutáneas? Descubra cómo la estabilización previene las úlceras por presión
- ¿Cómo contribuye el polvo cerámico de infrarrojos lejanos de alta pureza a la eficacia de los parches de fisioterapia de infrarrojos lejanos?